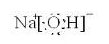氢氧化钠变质程度可通过以下方法检验,分为是否变质及完全/部分变质两种情况:
氢氧化钠变质是因与空气中二氧化碳反应生成碳酸钠(化学方程式:2NaOH + CO₂ = Na₂CO₃ + H₂O)。检测是否变质可通过以下三种溶液实现:
滴加稀盐酸(或稀硫酸)取少量样品于试管中,滴加稀盐酸,若产生气泡,说明已变质。原理:碳酸钠与酸反应生成二氧化碳气体(Na₂CO₃ + 2HCl = 2NaCl + CO₂↑ + H₂O),而氢氧化钠与酸反应无明显现象(NaOH + HCl = NaCl + H₂O)。
滴加氢氧化钙溶液(或氢氧化钡溶液)取少量样品于试管中,滴加氢氧化钙溶液,若产生白色沉淀,说明已变质。原理:碳酸钠与氢氧化钙反应生成碳酸钙沉淀(Na₂CO₃ + Ca(OH)₂ = CaCO₃↓ + 2NaOH),而氢氧化钠与氢氧化钙不反应。注意:氢氧化钡溶液也可用于检测,但后续检测完全/部分变质时需避免使用,因其会引入新的氢氧化钠干扰结果。
滴加氯化钡溶液(或其他可溶性钙盐、钡盐溶液)取少量样品于试管中,滴加氯化钡溶液,若产生白色沉淀,说明已变质。原理:碳酸钠与氯化钡反应生成碳酸钡沉淀(Na₂CO₃ + BaCl₂ = BaCO₃↓ + 2NaCl),而氢氧化钠与氯化钡不反应。替代试剂:硝酸钙、氯化钙等可溶性钙盐或钡盐溶液均可。
若需进一步判断氢氧化钠是完全变质(仅含碳酸钠)还是部分变质(含氢氧化钠和碳酸钠),可采用以下步骤:
步骤1:加入过量氯化钡溶液取少量样品于试管中,滴加过量氯化钡溶液,充分反应后静置。目的:完全除去溶液中的碳酸钠(生成碳酸钡沉淀和氯化钠),避免其对后续检测的干扰。原理:Na₂CO₃ + BaCl₂ = BaCO₃↓ + 2NaCl。注意:不可使用氢氧化钡溶液,因其会与碳酸钠反应生成新的氢氧化钠(Na₂CO₃ + Ba(OH)₂ = BaCO₃↓ + 2NaOH),影响对原氢氧化钠的检测。
步骤2:滴加酚酞溶液向上层清液中滴加少量酚酞溶液,观察颜色变化:
若溶液变红:说明溶液中仍含氢氧化钠,为部分变质。
若溶液不变红:说明溶液中无氢氧化钠,为完全变质。原理:氢氧化钠溶液呈碱性,能使酚酞变红;而碳酸钠被完全除去后,溶液若仍显碱性,则源于未变质的氢氧化钠。
皮肤接触:浓溶液会腐蚀表皮,造成烧伤。
眼部接触:0.02%溶液可损伤角膜上皮,溅入眼内可能导致深层组织损伤甚至失明。
吸入危害:粉尘刺激眼和呼吸道,腐蚀鼻中隔。
误食危害:导致消化道灼伤、呕吐、腹泻、吞咽困难,严重时可致休克或消化道穿孔。
环境危害:强碱性会污染水质,对植物和水生生物造成影响。